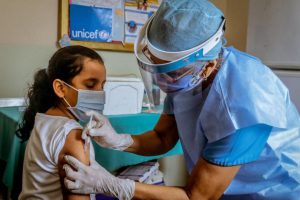
Para administrar una vacuna en niños, deben cumplirse tres pasos: consentimiento informado del representante, aval por escrito del niño mayor de 7 años y aprobación del Comité de Bioética para la Investigación. Si alguno de ellos falla, puede suspenderse la administración del fármaco
Transparencia Venezuela, 26 de octubre de 2021.- Las comunidades científicas del país no están en desacuerdo con la vacunación anti-COVID-19 en niños y adolescentes. Pero sí piden a las autoridades sanitarias aplicar vacunas reconocidas científicamente y que cuenten con estudios que demuestren la eficacia en personas mayores de 18 años.
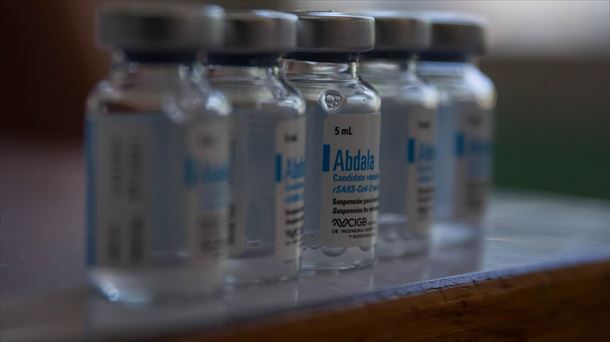
A propósito del anuncio de la vicepresidenta ejecutiva Delcy Rodríguez de comenzar la inmunización en mayores de 2 años edad, la Sociedad Venezolana de Puericultura y Pediatría señaló que el Estado no debe administrar vacunas sin bases científicas, como es el caso de las candidatas vacunales Abdala y Soberana 02, desarrolladas en Cuba. A pesar de que el Centro para el Control Estatal de Medicamentos, Equipos y Dispositivos Médicos de Cuba ha aprobado ambas para uso de emergencia, se desconocen los resultados de los ensayos clínicos en sus tres fases, por lo que están en entredicho su eficacia y seguridad, tanto en adultos como en la población pediátrica.
Según la agencia regulatoria cubana, la Soberana 02 puede aplicarse en personas entre 2 y 18 años de edad porque «cumple con los requisitos exigidos en cuanto a calidad, seguridad e inmunogenicidad para este grupo poblacional». Sin embargo, no hay evidencias de esta aseveración.
Leer más: Venezuela recibe 900.000 dosis de Abdala
El Centro Nacional de Bioética (Cenabi-Venezuela) emitió el cuarto comunicado relacionado con el uso de Abdala en niños y adolescentes. Este 25 de octubre insistieron en que Venezuela no debe asumir que se trata de una vacuna segura porque el centro de regulación de Cuba así lo considera. En este caso, le correspondería a la Junta Revisora de Productos Farmacéuticos, con sede en el Instituto Nacional de Higiene Rafael Rangel, determinar si es apta su aplicación en Venezuela.
«Los niños son considerados la población más vulnerable por sus condiciones biológicas relacionadas con su inmadurez de grado inverso a la edad, razón por la cual, el uso de nuevos fármacos y productos biológicos en ellos, debe estar precedido por la demostración de su eficacia e inocuidad en adultos, con la única excepción, de aquellos que estén dirigidos a problemas de salud propios de la infancia. En países con planes de vacunación bien estructurados y avanzados, se está comenzando a vacunar a menores en orden decreciente de edad, pero nunca incluyendo de entrada a niños tan pequeños y utilizando vacunas de eficacia e inocuidad demostradas», señala el centro.
Leer más: «Venezuela no debe aplicar Abdala en niños sin tener resultados de ensayos clínicos en adultos»
Además, indica el Cenabi que para aplicar una dosis de vacuna a un niño o adolescente deben cumplirse tres pasos: consentimiento informado firmado por el representante, aceptación del niño mayor de 7 años expresada en un asentimiento informado y aprobación del Comité de Bioética para la Investigación. «La falta de cualquiera de estas tres autorizaciones es suficiente para impedir la aplicación del producto», sentencia Cenabi.
Comunicado sobre vacunación en niños 25-10-21
El Ejecutivo no ha sido oportuno en publicar información sobre la aplicación de Abdala. Al país han llegado más de un millón de dosis de este prototipo cubano, pero solo se ha conocido del uso de 30.000 dosis para cumplir el esquema de 10.000 habitantes del complejo militar Fuerte Tiuna, ubicado en Caracas.
Hasta este 26 de octubre, la vacunación en adolescentes (12 a 17 años de edad) ha comenzado en al menos cinco estados: Vargas, Trujillo, Miranda, Bolívar y Delta Amacuro. Sin embargo, las dosis aplicadas son de la marca Sinopharm que, de acuerdo con una publicación de la revista científica The Lancet, en septiembre de este año, son seguras para la población entre 3 y 17 años.